文章分享吸附的定義、原理、分類(物理吸附與化學吸附)及關鍵影響因素(吸附質性質、表面特性、溫度、壓力、pH值)。閱讀本文,你可掌握吸附的基本機制、區別物理與化學吸附的關鍵特征,了解如何優化吸附過程,適用于化工、環保、材料等領域應用。
什么是吸附?
吸附(adsorption)是指物質在表面或界面上積聚并附著的現象,它涉及物質之間相互作用力的形成,通常發生在固體、液體或氣體的表面。這一過程是物質在界面上與其它物質的相互作用的結果,廣泛應用于化學工程、環境科學、生物學等領域。
吸附不僅僅是一種物理現象,它還可以通過化學作用力的介入形成更為復雜的吸附過程。因此,吸附現象可以通過物理吸附和化學吸附兩種主要類型進行詳細討論。
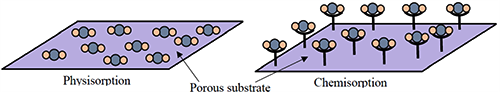
圖1.氣體分子與吸附劑表面在物理吸附和化學吸附過程中的相互作用示意圖。
吸附的原理吸附過程的本質涉及到吸附質分子與吸附表面分子之間的相互作用,通常表現為分子或原子在界面上的聚集。吸附質的吸附力可能源自范德瓦爾斯力、電場力、氫鍵等物理作用,也可能是由共價鍵、離子鍵等化學作用力所主導。
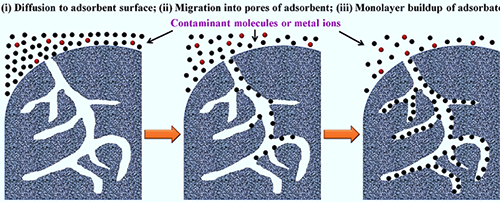
圖2.多孔材料吸附流程圖:(i)表面接觸(外擴散),(ii)吸附(內擴散),(iii)單分子層吸附平衡。
吸附的分類根據吸附質與吸附表面之間作用力的性質,吸附可以分為兩種主要類型:物理吸附和化學吸附。
物理吸附
物理吸附,也稱為范德瓦爾斯吸附,是由于吸附質分子與吸附表面之間存在弱的范德瓦爾斯力或偶極力等物理作用力而發生的吸附過程。該過程通常是可逆的,并且不涉及化學鍵的形成。
在物理吸附過程中,吸附質分子和表面之間的相互作用較弱,因此通常需要較低的溫度和壓力才能實現吸附。當外部條件發生變化時,吸附質容易被脫附回到氣相或溶液中。
物理吸附的特點是吸附量隨著溫度的升高而減小,反之則增加,且通常是單層吸附。物理吸附的一個重要特征是吸附過程的熱力學可逆性,且吸附能量較低。
化學吸附
化學吸附,也稱為化學結合吸附,是由于吸附質分子與吸附表面之間形成較強的化學鍵,如共價鍵、離子鍵等。該過程通常是不可逆的,并且具有較高的吸附能量。在化學吸附過程中,吸附質分子和表面之間的相互作用比物理吸附更強,因此化學吸附通常需要較高的能量(如較高的溫度或壓力)才能發生。
化學吸附的特點是吸附質和表面之間的相互作用是通過化學反應或者離子交換等方式實現的,通常涉及電子轉移或原子重排等復雜過程。化學吸附不僅需要較高的溫度和壓力條件,而且吸附量可能會隨著溫度升高而增加,但其過程的可逆性較差
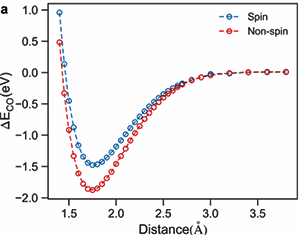
圖3.CO在Co表面化學吸附的勢能曲線示意圖。
物理吸附與化學吸附的區別
物理吸附和化學吸附的主要區別在于它們的吸附機制和能量來源。
物理吸附主要依賴于分子間的弱相互作用力,如倫敦色散力、誘導偶極力和偶極-偶極力等,這些作用力的強度較弱,因此吸附過程通常是可逆的,并且不涉及化學鍵的形成。相比之下,化學吸附是由于吸附分子和表面之間形成化學鍵(如共價鍵或離子鍵),這通常是不可逆的,吸附能較高,可以達到幾萬焦耳每摩爾。
物理吸附的吸附能較低,通常在幾千焦耳每摩爾的量級。因此,物理吸附過程對溫度變化較為敏感,吸附物質容易脫附。而化學吸附的過程涉及更強的能量變化,因此不太受溫度影響。
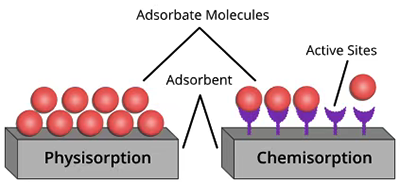
圖4.物理吸附與化學吸附的直觀對比示意圖。
影響吸附的因素
吸附過程受到多個因素的影響,這些因素決定了吸附的程度和速率。主要影響因素包括吸附質的性質、吸附表面的性質、溫度、壓力、溶液的pH值等。
①吸附質的性質
吸附質的分子量、極性、分子結構以及其與吸附表面相互作用的能力是影響吸附的首要因素。較大分子量的吸附質通常會在表面形成較大的吸附層,而極性較強的分子則會通過電場作用或氫鍵與表面發生較強的相互作用。此外,分子內部的官能團如羥基、氨基等也會增加吸附質與表面之間的化學相互作用,從而改變吸附性能。
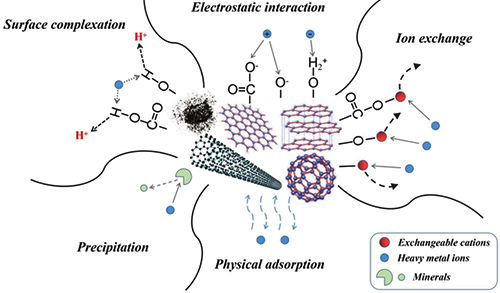
圖5.重金屬在碳基官能團吸附劑上的吸附機制示意圖。
②吸附表面的性質
吸附表面的性質對于吸附過程至關重要。表面的比表面積越大,能夠提供的吸附位點越多,吸附量通常也越大。
表面的化學成分、表面能和表面粗糙度也會對吸附過程產生影響。具有較高比表面積的材料,如活性炭、納米材料等,通常具有較高的吸附能力。表面上的官能團也會通過提供額外的吸附位點來提高吸附效率。
③溫度
溫度是影響吸附過程的一個重要因素。在物理吸附過程中,隨著溫度升高,吸附質的分子運動加劇,導致吸附質與表面之間的弱相互作用減弱,吸附量通常會減小。
反之,化學吸附則可能隨著溫度的升高而增強,因為化學反應的速率常常隨著溫度升高而加速。然而,過高的溫度也可能破壞吸附質與表面之間的化學鍵,導致吸附過程不可逆。
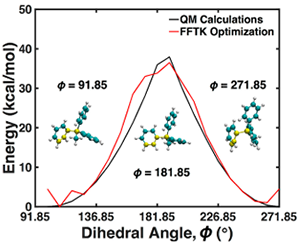
圖6.MePh3P?中C–C–C–P二面角(黃色原子)在Φ=91.85°至271.85°范圍內以15°為步長變化時的能量面比較。
④壓力
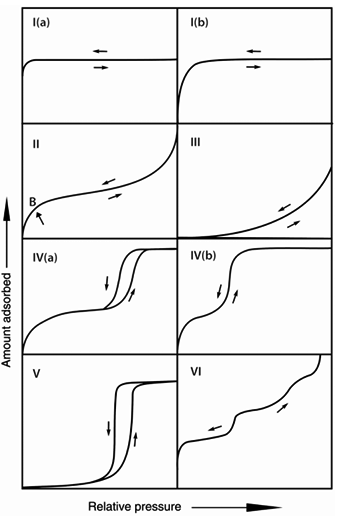
吸附質的濃度與其在氣相中的壓力密切相關。在氣體吸附中,隨著氣體壓力的增大,吸附量通常會增加,直到達到吸附表面的飽和狀態。這一現象在Langmuir吸附等溫線中得到了廣泛的描述。對于液體中的吸附過程,溶解度的增加通常伴隨著吸附量的增大。
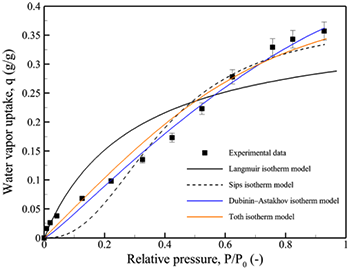
圖7.硅膠在30°C下的平衡吸附等溫線示意圖。
⑤溶液的pH值
在液相吸附過程中,溶液的pH值對吸附過程也有顯著影響。不同的pH值可能會改變吸附質的電荷性質以及吸附表面的電荷分布,進而影響吸附過程。酸性或堿性環境下,吸附質的離子化程度不同,這可能導致吸附效能的變化。







